عنـوان الوحدة6 :الحموض والقواعد
Properties of Acids
للحموض صفات عامة، منها:
1- للحموض الموجودة في المواد الغذائية طعم حمضي (لاذع).
2- تغير لون ورقة تباع الشمس الزرقاء إلى اللون الأحمر.
3- توصل محاليها المائية التيار الكهربائي.
4- تبدأ أسماؤها بكلمة حمض، مثل حمض الهيدروكلوريك.
استخدامات الحموض
Uses of Acids
الجدول التالي يمثل عدداً من الحموض، وأماكن وجودها، واستخداماتها:
خصائص القواعد
Properties of Bases
للقواعد صفات عامة، منها:
1- للقواعد الموجودة في المواد الغذائية طعم مرّ.
2- ملمسها صابوني.
3- تغير لون ورقة تباع الشمس الحمراء إلى اللون الأزرق.
4- توصل محاليها المائية التيار الكهربائي.
5- تبدأ أسماؤها بكلمة هيدروكسيد يتبعها اسم العنصر؛ مثل:
هيدروكسيد الصوديوم، وهيدروكسيد الكالسيوم.
استخدامات القواعد
Uses of Bases
تستخدم القواعد بشكل واسع في مواد التنظيف.
الجدول التالي يمثل عدداً من القواعد، واستخداماتها:
مضادات الحموضة
يوجد في المعدة حمض الهيدروكلوريك، والذي يُساعد على هضم الطعام.
يعاني البعض من زيادة حموضة المعدة، لذا ينصحهم الأطباء بتناول مضادات الحموضة، وهي مواد تحتوي على هيدروكسيد المغنيسيوم (قاعدة)؛ لتعمل على معادلة حموضة المعدة، والتقليل من أعراض سوء الهضم الحمضي.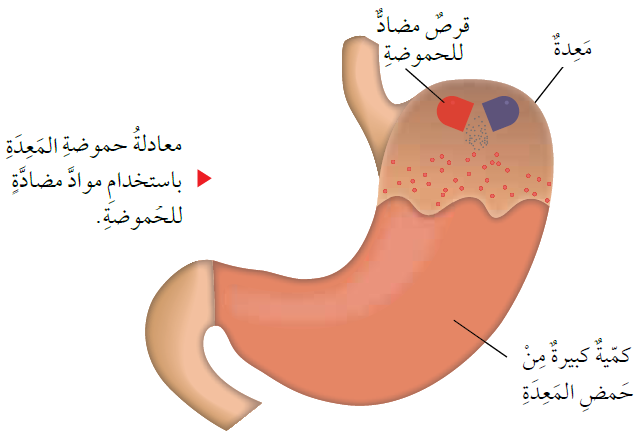
أسئلة المحتوى وإجاباتها
خصائص الحموض والقواعد
أتأمل الصورة صفحة (8):
تختلف الثمار في ألوانها وطعمها؛ لاحتوائها على مركبات كيميائية تُكسبها تلك الخصائص، وتتميز الحمضيات مثل الليمون والبرتقال بطعمها اللاذع. فما سبب الطعم اللاذع للحمضيات؟
سبب الطعم اللاذع للحمضيات هو وجود مركبات تُسمى الحموض؛ لذا، يُطلق على الليمون والبرتقال اسم الحمضيات.
أستكشف صفحة (9):
تنصيف المحاليل إلى حمضية وقاعدية
التفكير الناقد: أفسر عدم تغير لون ورقتي تباع الشمس الحمراء والزرقاء؛ عند إضافة قطرة من محلول ملح الطعام إليهما.
محلول ملح الطعام لا يحمل خصائص حمضية ولا خصائص قاعدية؛ لذا، لم يؤثر في لون ورقتي تبّاع الشمس الحمراء والزرقاء.
أتحقق صفحة (10):
لماذا يجب الحذر عند استخدام هيدروكسيد الصوديوم؟
لأن هيدروكسيد الصوديوم مادة كاوية للجلد.
أتحقق صفحة (11):
أذكر خصائص الحمض.
مواد لها طعم حمضي، تغير لون ورقة تباع الشمس الزرقاء إلى اللون الأحمر، ومحاليلها موصلة للتيار الكهربائي، والصناعية منها كاوية للجلد وتتلف بعض المواد.
أتحقق صفحة (12):
أنظم جدولاً يتضمن الحموض في المواد المألوفة لدي واستخداماتها.
أتحقق صفحة (13):
ما خصائص القواعد.
القواعد مواد لها طعم مرّ، وملمسها صابوني، تغير لون ورقة تباع الشمس الحمراء إلى اللون الأزرق، ومحاليلها توصل التيار الكهربائي، وبعضها تبدأ أسماؤها بكلمة هيدروكسيد يتبعها اسم الفلز، وهي كاوية للجلد.
أفكر صفحة (14):
ماذا يمكن أن يحدث لنباتات مزروعة في تربة حموضتها قليلة إذا أضفتُ إلى التربة هيدروكسيد الكالسيوم؟
هيدروكسيد الكالسيوم من القواعد، وإذا أضفتها إلى التربة تقل حموضتها؛ ما يحسن إنتاج المزروعات.
أتحقق صفحة (15):
أذكر تطبيقات على استخدامات القواعد.
تجربة صفحة (15):
الكشف عن حمضية أو قاعدية مسحوق الخبيز
التحليل والاستنتاج:
أفسر: تغير لون ورقة تبّاع الشمس؛ عند إضافة مسحوق الخبيز إليها.
يتغير لون ورقة تبّاع الشمس الحمراء إلى اللون الأزرق؛ لأن مسحوق الخبيز مادّة قاعدية التأثير.
أسئلة مراجعة الدرس الأول
خصائص الحموض والقواعد
السؤال الأول:
الفكرة الرئيسة: أوضّح أهمية الحموض والقواعد.
السؤال الثاني:
أعدد (3) أمثلة لحموض و (3) أمثلة لقواعد مألوفة في حياتي اليومية.
السؤال الثالث:
أقارن بين المحاليل الحمضية والمحاليل القاعدية من حيث: الطعم، والتوصيل الكهربائي.
السؤال الرابع:
أصف كيف يمكنني استخدام ورقة تباع شمس حمراء للتمييز بين الحمض والقاعدة.
السؤال الخامس:
أفسّر ما يأتي:
أ- ارتداء النظارة الواقية والقفافيز؛ عند تسميد التربة.
ب- لا يمكنني التمييز بين الحموض والقواعد بالتذوق.
السؤال السادس:
أصوغ فرضيتي: أنبوبا اختبار يحتوي أحدهما على محلول حمض الهيدروكلوريك والآخر على محلول هيدروكسيد الصوديوم، ولكن الملصق الذي يحمل اسم كل منهما مفقود. كيف يمكنني تحديد محتوى كل أنبوب، وكتابة اسمه على الملصق الخاص به.
السؤال السابع:
التفكير الناقد: يُنصح بتنظيف الأسنان باستمرار للمحافظة عليها من النخر. أتوقع سبب حدوث النخر في الأسنان.
Indicators
كيف يمكنك التمييز عملياً بين محاليل الحموض، ومحاليل القواعد؟
لا يمكن التمييز بين محاليل الحموض ومحاليل القواعد بالتذوق؛ لأن محاليل الحموض والقواعد كاوية وحارقة؛ وذلك خطر جداً.
للتميز بين الحموض والقواعد نستخدم مواد تعرف بالكواشف.
مفهوم الكواشف
الكواشف: مواد يتغير لونها تبعاً لنوع المحلول الذي تكون فيه.
تمتاز الكواشف بأنها تعطي لوناً في محاليل الحموض يختلف عن اللون الذي تعطيه في محاليل القواعد.
أنواع الكواشف
تقسم الكواشف حسب مصدرها إلى نوعين، هما:
أولاً: الكواشف الطبيعية
الكواشف الطبيعية: مواد تستخلص من مواد طبيعية مثل: أوراق الشاي والملفوف الأحمر وبتلات الورد الجوري.
أمثلة:
يعتبر الشاي ومنقوع الملفوف الأحمر كواشف طبيعية، انظر لون محلول كل منهما عند إضافة كل من عصير الليمون (تأثيره حمضي)، أوراق الميرمية (تأثيرها قاعدي) إليهما:
ثانياً: الكواشف الصناعية
الكواشف الصناعية: مواد تحضر صناعياً ويتغير لونها تبعاً لنوع المحلول الذي تُضاف إليه وبعضها على صورة أوراق، منها أوراق تباع الشمس الحمراء والزرقاء.
الرقم الهيدروجيني (pH)
Power of Hydrogen (pH)
يعبر عن حمضية أو قاعدية المحاليل برقم يُعرف بالرقم الهيدروجيني (pH).
يعبر عن الرقم الهيدروجيني بتدريج رقمي يتراوح بين (14-0) ويُسمى تدريج الرقم الهيدروجيني.
تصنيف المحاليل حسب قيم (pH)
الكاشف العام
Universal Indicator
يمكن قياس قيمة الرقم الهيدروجيني (pH) للمحاليل عملياً بإحدى طريقتين:
1- الكاشف العام
الكاشف العام: مزيج من عدّة كواشف يكون في صورة سائل أو أشرطة ورقية، ويُستخدم في تقدير قيمة الرقم الهيدروجيني للمحلول الحمضي أو القاعدي. يرفق مع الكاشف العام دليل ألوان قياسي أحياناً، يكون ملصقاً على العلبة التي يوجد فيها.
2- جهاز قياس الرقم الهيدروجيني
جهاز مقياس الرقم الهيدروجيني: جهاز يُستخدم لقياس الرقم الهيدروجيني في المختبرات، وفي العديد من الصناعات الكيميائية التي تعتمد على حمضية المحاليل وقاعديتها.
أسئلة المحتوى وإجاباتها
الكواشف والرقم الهيدروجيني
أتحقق صفحة (18):
ما أنواع الكواشف؟ أذكر مثالاً على كلّ منها.
تجربة صفحة (18):
تصنيف الكواشف
التحليل والاستنتاج:
1- أقارن بين منقوع الملفوف الأحمر وورق تباع الشمس من حيث: مصدر كل منهما، وتأثير إضافة الحمض والقاعدة في لونهما.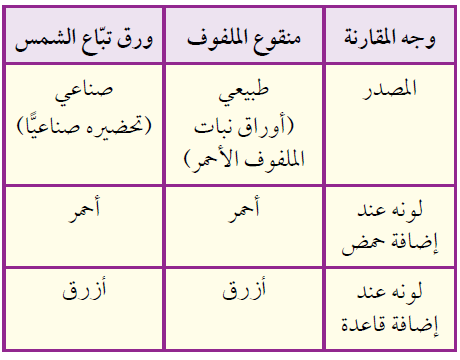
2- أفسر: أستخدم عينة ضابطة في التجربة.
أستخدم عينة ضابطة في التجربة؛ لأنها تعدّ مرجعاً لمقارنة لون المحلول المراد اختباره، بلون المحاليل المحدد نوعها حمضية أم قاعدية.
أتحقق صفحة (19):
ما المقصود بالرقم الهيدروجيني pH ؟
الرقم الهيدروجيني هو مقياس لحمضية أو قاعدية المحاليل، ويعبر عنه بتدريج رقمي من (14-0).
أفكر صفحة (20):
ما الأسباب التي تؤدي إلى تغير قيمة pH لدم الإنسان؟
هنالك أسباب متعددة تؤدي إلى تغير قيمة pH لدم الإنسان، منها بعض الحالات المرضية كالأمراض التنفسية، كما أن بعض الأدوية تسبب تغير قيمة الرقم الهيدروجيني للدم.
أتحقق صفحة (20):
أفسر لمَ يُعدّ جهاز مقياس الرقم الهيدروجيني، أكثر دقة من الكاشف العام.
يُعدّ جهاز مقياس الرقم الهيدروجيني، أكثر دقة من الكاشف العام؛ لأنه يحدد درجة حمضية المحلول ومدى ملاءمة استخدامه في مجال ما.
تجربة صفحة (21):
استخدام الكاشف العام
التحليل والاستنتاج:
1- أرتب المواد تصاعدياً حسب قيم pH .
حمض الهيدروكلوريك المخفف، الخل، عصير الليمون، ماء مقطر، محلول مسحوق الخبيز، محلول منظف الزجاج، محلول هيدروكسيد الصوديوم.
2- أصنّف المواد إلى حمضية وقاعدية ومتعادلة.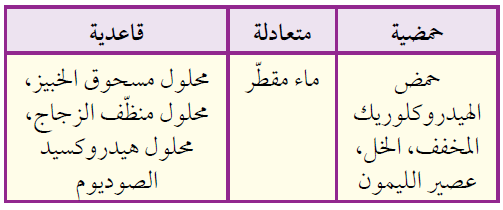
3- أقارن بين الكاشف العام والكواشف الأخرى.
الكاشف العام يحدد درجة حمضية أو قاعدية المحلول.
أسئلة مراجعة الدرس الثاني
الكواشف والرقم الهيدروجيني
السؤال الأول:
أفسّر. تُستخدم الكواشف للتمييز بين الحموض والقواعد.
السؤال الثاني:
أصنف المحاليل الآتية إلى حمضية أو قاعدية أو متعادلة بناءً على قيم pH :
أ- المحلول (أ): pH = 3
ب- المحلول (ب): pH = 8
ب- المحلول (د): pH = 7
السؤال الثالث:
أستنتج مستعيناً بقيم pH على تدريج الرقم الهيدروجيني في الشكل المجاور، أيّ الجمل الآتية صحيحة وأيّها غير صحيحة؟
أ- المحاليل الأكثر حمضية؛ قيم pH لها تقترب من 7 .
ب- المحاليل الأكثر قاعدية؛ قيم pH لها أكبر من 7 .
ج- يمكن تحديد الرقم الهيدروجيني للمحلول؛ باستخدام ورقة تباع الشمس.
السؤال الرابع:
التفكير الناقد: عند اختبار عينة من الحليب باستخدام ورقة تباع الشمس الزرقاء بقي لونها أزرق، وعند ترك الحليب لمدة من الزمن وإعادة الاختبار، وجد أن لون ورقة تباع الشمس الزرقاء تحول إلى اللون الأحمر. ما توقعاتي للتغيرات التي حدثت للحليب؟
تطبيق الرياضيات
مستعيناً بقيم pH على تدريج الرقم الهيدروجيني في الشكل السابق، أحسب مقدار الرقم الهيدروجيني pH لمحلول ما، علماً بأن مقداره يقل عن مثلي الرقم الهيدروجيني للماء بثلاثة أمثال الرقم الهيدروجيني لثمرة ليمون.
الإثراء والتوسّع
أزهار نبات القرطاسيا
تختلف ألوان أزهار نبات القرطاسيا تبعًا لدرجةِ حُموضة التربة، وقد استفاد المزارعونَ مِنْ هذه الظاهرة في إنتاج هذا النباتِ بألوان أزهار مختلفة؛ وذلك بإضافة مواد تعمل على تغيير قيمة الرقم الهيدروجيني للتربة التي ينبتُ فيها، فغيّروا لونَها مِنَ الزهري إلى الأزرق بناءً على امتصاص النبتة للمادة المضافة. أنظر الشكل (15).
أبحــث فــي مصادر المعرفة المتاحة، عــن المـواد التي يمكنني إضافتها للتربـة لإنتاج أزهار القرطاسيا ذاتِ اللون الزهري أو الأزرق، وأتعاون مع زملائي على زراعة أزهار القرطاسيا بألوانها المختلفة في حديقة مدرستي.
يتصف نبات القرطاسيا بأزهاره التي تتوضع في كتل كروية على شكل باقة عديمة الرائحة. ويمكن التحكّم بلون الأزهار عن طريق التحكم بدرجة حموضة التربة التي ينمو فيها. فقد وجد أنه يُمكن إضافة سلفات الألمنيوم مع مياه الري لتصبح التربة قاعدية؛ وبذا يتغيّر لون أزهار النبات ليصبح أزرق.
أنظر إلى الملف المرفق والذي يبين كيف يمكن تتغير لون أزهار نبات القرطاسيا من كتاب الكيمياء للصف الثاني عشر.
استقصاء علمي
تأثير المطر الحمضي في إنبات البذور
سؤال الاستقصاء:
تحتاج عملية إنبات البذور إلى الماء الذي تمتصه الجذورُ مِنَ التربة، ومن أهم مصادره مياه الأمطار التي تُعدُّ مِنَ المحاليل الحمضية الضعيفة؛ لأنها تحتوي على غاز ثاني أكسيد الكربون CO الذي يتفاعل مع بخار الماء في الهواء الجوي فيتكونُ حَمضُ الكربونيك، وتزداد حمضية ماء المطر بانخفاض قيمة الرقم الهيدروجيني pH فهل يؤثر التغير في قيمة الرقم الهيدروجيني للمياه في عملية إنبات البذور ؟
التحليل والاستنتاج والتطبيق
1- أفسّر استخدامي ملوّنَ طعام في أنبوب الاختبار (1) في الجزء (A)؟
استخدم الصبغة الملوّنة لتوضيح الملاحظة؛ لأنّ محلول الخل الأبيض شفّاف، ولون المحاليل يختلف باختلاف التركيز .
2- أحدّدُ المتغترات التابعة والمتغيّرات المستقلة في التجربة في الجزء (A) والجزء (B)؟
المتغيرات المستقلة في الجزء (A): درجة الحرارة وحجم المحلول، والتابعة هي الرقم الهيدروجيني. المتغيّرات المستقلة في الجزء (B): نوع البذور وحجم المحلول، والتابعة هي معدل إنبات البذور.
3- أُقدم دليلًا على حدوث عملية إنبات البذور.
الدليل على إنبات البذور ظهور الجذور للبذور.
4- ماذا تمثل المحاليل التي أضفتها للبذور ؟
مياه المطر.
5- أستخدم الأرقام: أحسبُ النسبة المئوية للبذور التي حدثت لها عملية إنبات في كُلِّ علبة،
وأُدوّنُ نتائجي.
تحقق من حسابات الطلبة للنسب المئوية وفقا لنتائجهم.
6- أُمثْلُ بيانيًا العلاقة بين قيمة الرقم الهيدروجيني (pH) للمحلول، والنسبة المئوية للبذور التي حدث لها إنبات.
تكون العلاقة عكسية بين معدل إنبات البذور وقيمة الرقم الهيدروجيني (كلّما قل الرقم الهيدروجيني للماء الذي تمتصه الجذور، زادت حمضية التربة فيقل معدل انبات البذور.
7- أُقارن نتائجي بصحة الفرضية التي كوّنتها.
وافقت نتائجي توقعاتي وثبت بالتجربة العملية أنّ الرقم الهيدروجيني يؤثر في إنبات البذور، وأنه كلّما قل الرقم الهيدروجيني (زادت حمضية مياه المطر)، قل معدل إنبات البذور.
إجابات أسئلة مراجعة الوحدة
السؤال الأول:
أكتب المفهوم العلمي المناسب لكل جملةٍ من الجمل الآتية:
السؤال الثاني:
أختار رمز الإجابة الصحيحة في ما يأتي:
1- إحدى المواد الآتية تغير لون ورقة تباع الشمس الحمراء إلى اللون الأزرق:
أ- ملح الطعام.
ب- سائل التنظيف.
ج- الخل.
د- الشاي.
2- الخاصية التي تشترك فيها محاليل الحموض والقواعد، هي:
أ- طعمها حامض.
ب- ملمسها صابوني.
ج- موصلة للتيار الكهربائي.
د- آكلة لبعض الفلزات.
3- معظم المواد التي تُستخدم في صناعة مواد التنظيف، هي:
أ- قاعدية.
ب- حمضية.
ج- أملاح.
د- متعادلة.
4- محلول الحمض الذي يُسهم في عملية هضم الطعام في المعدة، هو:
أ- حمض النيتريك.
ب- الكبريتيك.
ج- الهيدروكلوريك.
د- الخل.
5- يشير الرمز المجاور عند وجوده على ملصقات إحدى المواد إلى أنها:
أ- سامة.
ب- قابلة للاشتعال.
ج- كاوية للجلد.
د- تسبب الجروح.
6- السبب الرئيس لحدوث المطر الحمضي:
أ- النفايات الناتجة من الطاقة النووية.
ب- الانسكابات من مصانع المواد الكيماوية.
ج- الغازات الناتجة من احتراق الوقود الأحفوري.
د- الغازات المنبعثة من علب المعطرات الجوية.
7- قيمة pH للماء النقي، تساوي:
أ- 3
ب- 0
ج- 7
د- 9
8- يُصنف محلول مادة ما، قيمة pH له = 14 بأنه:
أ- مادة قاعدية.
ب- مادة حمضية.
ج- مادة متعادلة.
د- مطر حمضي.
9- الجهاز المستخدم في قياس درجة حموضة ماء المطر بدقة، هو:
أ- الميزان الزئبقي.
ب- مقياس درجة الحرارة.
ج- الميزان الحساس.
د- مقياس الرقم الهيدروجيني.
10- عند سقوط قطرات من عصير الليمون على سطح من الصخر الجيري، ينتج غاز:
أ- H2
ب- O2
ج- CO2
د- N2
السؤال الثالث:
المهارات العلمية
1- أكمل خريطة المفاهيم الآتية: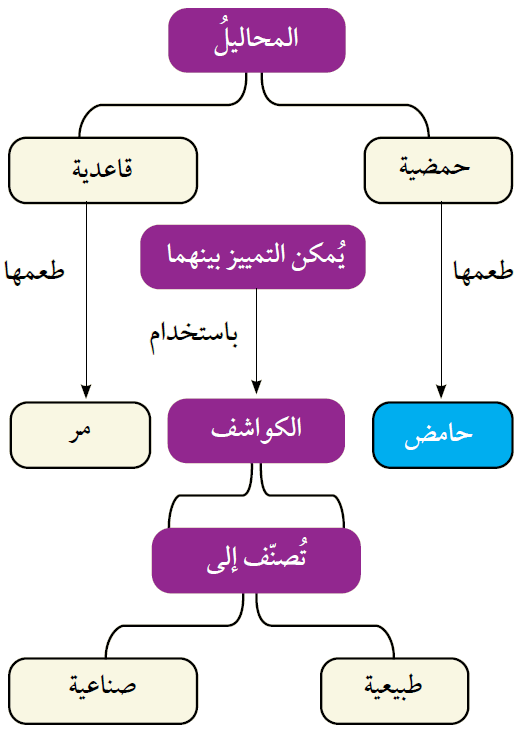
2- أصنف المواد الافتراضية (س، ص، ع، ل) إلى حمض أو قاعدة؛ مستعيناً بالمعلومات الواردة في الجدول الآتي: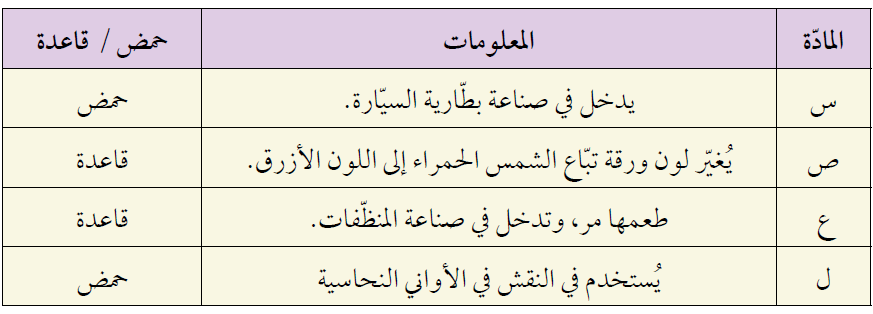
3- أفسّر الظواهر الآتية بناءً على مفهومي للحموض والقواعد والكواشف:
أ- تستخدم مادة قاعدية في صناعة معجون الأسنان.
للتخلص من المواد الحمضية التي تبقى بعد تناول الطعام بين الأسنان، التي يمكن أن تسبب نخر الأسنان.
ب- تكون الكهوف الجيرية، مثل مغارة برقش في الأردن.
بسبب المطر الحمضي الذي يتفاعل مع كربونات الكالسيوم، ويتصاعد منها غاز ثاني أكسيد الكربون، ما أدى إلى وجود الكهوف الجيرية.
ج- ارتداء القفافيز في أثناء استخدام مواد التنظيف.
لأن مواد التنظيف تدخل في تركيبها مواد قاعدية وهي كاوية للجلد.
4- أصف دور مضاد الحموضة في تخفيف الحموضة في المعدة.
يُستخدم هيدروكسيد المغنيسيوم مضاداً لحموضة المعدة، إذ إنّه مادة قاعدية تتفاعل مع الزيادة في المحلول الحمضي في المعدة وتعادله، ما يخفف من أعراض سوء الهضم الحمضي.
5- ينتج من احتراق الفحم الحجري في بعض محطات توليد الطاقة غاز ثاني أكسيد النيتروجين. أصف تأثير هذه العملية في المباني القريبة من هذه المحطات.
نتيجة احتراق الوقود الأحفوري (مشتقات النفط) تنتج غازات مثل NO2 التي تتفاعل مع ماء المطر الحمضي، وعند سقوطه على المباني المكونة من الحجر الجيري أو الرملي التي تتكون من كربونات الكالسيوم CaCO3 ؛ تعمل على إذابة جزء منها ويتصاعد غاز CO2 وتصبح المباني مشوهة.
6- مستعيناً بالشكل والجدول الآتيين، أجيب عن الأسئلة الآتية:
أ- أستنتج: ما المواد التي استخدمها في حياتي اليومية تمثل الرموز (أ، ب، ج، د، هـ)؟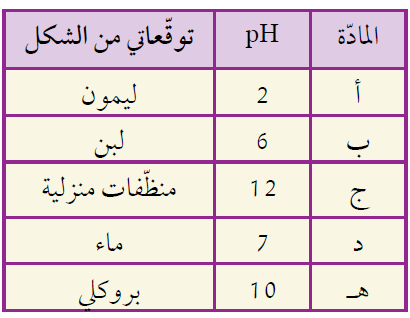
ب- أتوقع: ما المواد الغذائية التي يمكن تناولها للتخفيف من حموضة المعدة؟
يمكن استخدام البروكلي لتخفيف حموضة المعدة.
ج- أتوقع: ماذا يمكن أن يحدث لسطح الرخام إذا قطعت الليمون عليه باستمرار؟
تقطيع الليمون على سطح الرخام باستمرار يؤدي إلى تلفه وتشوه سطحه وتكوين حفر فيه؛ نتيجة تفاعل الحمض مع كربونات الكالسيوم المكون الكيميائي للرخام، ويتصاعد غاز CO2 ، فتتكون الحفر ويتشوه الرخام.
الدرس الأول: خصائص الحموض والقواعد
مصطلحات ومفاهيم علمية
| الحمض | Acid |
| القاعدة | Base |
| لاذع (حامض) | Sour |
| مُرّ | Bitter |
خصائص الحموض
Properties of Acids
للحموض صفات عامة، منها:
1- للحموض الموجودة في المواد الغذائية طعم حمضي (لاذع).

2- تغير لون ورقة تباع الشمس الزرقاء إلى اللون الأحمر.

3- توصل محاليها المائية التيار الكهربائي.
4- تبدأ أسماؤها بكلمة حمض، مثل حمض الهيدروكلوريك.
استخدامات الحموض
Uses of Acids
الجدول التالي يمثل عدداً من الحموض، وأماكن وجودها، واستخداماتها:
| الحمض | مكان وجوده | استخداماته |
| الفوليك | الخضراوات الورقية | ضروري لنمو الخلايا |
| حمض الأسيتيك | الخل | يستخدم في الطعام |
| حمض الأسكوربيك (فيتامين C) | الحمضيات | الوقاية من الأمراض |
| الستريك | البندورة والحمضيات | |
| الكبريتيك | بطارية السيارة | صناعة الأسمدة، والبلاستيك، وبطاريات السيارات |
| الهيدروكلوريك | المعدة | تنظيف سطوح الأواني، هضم الطعام |
| النيتريك والفسفوريك | الأسمدة | تسميد التربة |
Properties of Bases
للقواعد صفات عامة، منها:
1- للقواعد الموجودة في المواد الغذائية طعم مرّ.
2- ملمسها صابوني.
3- تغير لون ورقة تباع الشمس الحمراء إلى اللون الأزرق.
4- توصل محاليها المائية التيار الكهربائي.
5- تبدأ أسماؤها بكلمة هيدروكسيد يتبعها اسم العنصر؛ مثل:
هيدروكسيد الصوديوم، وهيدروكسيد الكالسيوم.
استخدامات القواعد
Uses of Bases
تستخدم القواعد بشكل واسع في مواد التنظيف.
الجدول التالي يمثل عدداً من القواعد، واستخداماتها:
| القاعدة | استخداماتها |
| هيدروكسيد الصوديوم | صناعة الصابون |
| أكسيد الكالسيوم وهيدروكسيد الكالسيوم | تقليل حموضة التربة، لتحسين إنتاج المزروعات |
| هيدروكسيد المغنيسيوم | تخفيف حموضة المعدة، والتخفيف من أعراض سوء الهضم الحمضي |
يوجد في المعدة حمض الهيدروكلوريك، والذي يُساعد على هضم الطعام.
يعاني البعض من زيادة حموضة المعدة، لذا ينصحهم الأطباء بتناول مضادات الحموضة، وهي مواد تحتوي على هيدروكسيد المغنيسيوم (قاعدة)؛ لتعمل على معادلة حموضة المعدة، والتقليل من أعراض سوء الهضم الحمضي.

أسئلة المحتوى وإجاباتها
خصائص الحموض والقواعد
أتأمل الصورة صفحة (8):
تختلف الثمار في ألوانها وطعمها؛ لاحتوائها على مركبات كيميائية تُكسبها تلك الخصائص، وتتميز الحمضيات مثل الليمون والبرتقال بطعمها اللاذع. فما سبب الطعم اللاذع للحمضيات؟
سبب الطعم اللاذع للحمضيات هو وجود مركبات تُسمى الحموض؛ لذا، يُطلق على الليمون والبرتقال اسم الحمضيات.
أستكشف صفحة (9):
تنصيف المحاليل إلى حمضية وقاعدية
التفكير الناقد: أفسر عدم تغير لون ورقتي تباع الشمس الحمراء والزرقاء؛ عند إضافة قطرة من محلول ملح الطعام إليهما.
محلول ملح الطعام لا يحمل خصائص حمضية ولا خصائص قاعدية؛ لذا، لم يؤثر في لون ورقتي تبّاع الشمس الحمراء والزرقاء.
أتحقق صفحة (10):
لماذا يجب الحذر عند استخدام هيدروكسيد الصوديوم؟
لأن هيدروكسيد الصوديوم مادة كاوية للجلد.
أتحقق صفحة (11):
أذكر خصائص الحمض.
مواد لها طعم حمضي، تغير لون ورقة تباع الشمس الزرقاء إلى اللون الأحمر، ومحاليلها موصلة للتيار الكهربائي، والصناعية منها كاوية للجلد وتتلف بعض المواد.
أتحقق صفحة (12):
أنظم جدولاً يتضمن الحموض في المواد المألوفة لدي واستخداماتها.
أتحقق صفحة (13):
ما خصائص القواعد.
القواعد مواد لها طعم مرّ، وملمسها صابوني، تغير لون ورقة تباع الشمس الحمراء إلى اللون الأزرق، ومحاليلها توصل التيار الكهربائي، وبعضها تبدأ أسماؤها بكلمة هيدروكسيد يتبعها اسم الفلز، وهي كاوية للجلد.
أفكر صفحة (14):
ماذا يمكن أن يحدث لنباتات مزروعة في تربة حموضتها قليلة إذا أضفتُ إلى التربة هيدروكسيد الكالسيوم؟
هيدروكسيد الكالسيوم من القواعد، وإذا أضفتها إلى التربة تقل حموضتها؛ ما يحسن إنتاج المزروعات.
أتحقق صفحة (15):
أذكر تطبيقات على استخدامات القواعد.
- يستخدم هيدروكسيد المغنيسيوم في تركيب مضادات الحموض؛ إذا يخفف من حموضة المعدة، ويخفف من أعراض سوء الهضم.
- يُستخدم هيدروكسيد الأمونيوم في صناعة الأسمدة.
- يُستخدم هيدروكسيد الباريوم في تشحيم السيارات.
- يُستخدم هيدروكسيد البوتاسيوم في الزراعة.
- يُستخدم هيدروكسيد الصوديوم في صناعة الصابون ومواد التنظيف.
تجربة صفحة (15):
الكشف عن حمضية أو قاعدية مسحوق الخبيز
التحليل والاستنتاج:
أفسر: تغير لون ورقة تبّاع الشمس؛ عند إضافة مسحوق الخبيز إليها.
يتغير لون ورقة تبّاع الشمس الحمراء إلى اللون الأزرق؛ لأن مسحوق الخبيز مادّة قاعدية التأثير.
أسئلة مراجعة الدرس الأول
خصائص الحموض والقواعد
السؤال الأول:
الفكرة الرئيسة: أوضّح أهمية الحموض والقواعد.
السؤال الثاني:
أعدد (3) أمثلة لحموض و (3) أمثلة لقواعد مألوفة في حياتي اليومية.
السؤال الثالث:
أقارن بين المحاليل الحمضية والمحاليل القاعدية من حيث: الطعم، والتوصيل الكهربائي.
السؤال الرابع:
أصف كيف يمكنني استخدام ورقة تباع شمس حمراء للتمييز بين الحمض والقاعدة.
السؤال الخامس:
أفسّر ما يأتي:
أ- ارتداء النظارة الواقية والقفافيز؛ عند تسميد التربة.
ب- لا يمكنني التمييز بين الحموض والقواعد بالتذوق.
السؤال السادس:
أصوغ فرضيتي: أنبوبا اختبار يحتوي أحدهما على محلول حمض الهيدروكلوريك والآخر على محلول هيدروكسيد الصوديوم، ولكن الملصق الذي يحمل اسم كل منهما مفقود. كيف يمكنني تحديد محتوى كل أنبوب، وكتابة اسمه على الملصق الخاص به.
السؤال السابع:
التفكير الناقد: يُنصح بتنظيف الأسنان باستمرار للمحافظة عليها من النخر. أتوقع سبب حدوث النخر في الأسنان.
الدرس الثاني: الكواشف والرقم الهيدروجيني
الكواشفIndicators
كيف يمكنك التمييز عملياً بين محاليل الحموض، ومحاليل القواعد؟
لا يمكن التمييز بين محاليل الحموض ومحاليل القواعد بالتذوق؛ لأن محاليل الحموض والقواعد كاوية وحارقة؛ وذلك خطر جداً.
للتميز بين الحموض والقواعد نستخدم مواد تعرف بالكواشف.
مفهوم الكواشف
الكواشف: مواد يتغير لونها تبعاً لنوع المحلول الذي تكون فيه.
تمتاز الكواشف بأنها تعطي لوناً في محاليل الحموض يختلف عن اللون الذي تعطيه في محاليل القواعد.
أنواع الكواشف
تقسم الكواشف حسب مصدرها إلى نوعين، هما:
أولاً: الكواشف الطبيعية
الكواشف الطبيعية: مواد تستخلص من مواد طبيعية مثل: أوراق الشاي والملفوف الأحمر وبتلات الورد الجوري.
أمثلة:
يعتبر الشاي ومنقوع الملفوف الأحمر كواشف طبيعية، انظر لون محلول كل منهما عند إضافة كل من عصير الليمون (تأثيره حمضي)، أوراق الميرمية (تأثيرها قاعدي) إليهما:
| الكاشف الطبيعي | لونه في الوسط الحمضي | لونه في الوسط القاعدي |
| محلول الشاي | أصفر (تجعله فاتحاً) | أسود (تجعله غامقاً) |
| منقوع الملفوف الأحمر | أحمر | أخضر أو أزرق |
الكواشف الصناعية: مواد تحضر صناعياً ويتغير لونها تبعاً لنوع المحلول الذي تُضاف إليه وبعضها على صورة أوراق، منها أوراق تباع الشمس الحمراء والزرقاء.
الرقم الهيدروجيني (pH)
Power of Hydrogen (pH)
يعبر عن حمضية أو قاعدية المحاليل برقم يُعرف بالرقم الهيدروجيني (pH).
يعبر عن الرقم الهيدروجيني بتدريج رقمي يتراوح بين (14-0) ويُسمى تدريج الرقم الهيدروجيني.
تصنيف المحاليل حسب قيم (pH)
- المحاليل الحمضية: تكون قيم (pH) لها من (0 إلى أقل من 7)، والمحاليل الأقرب إلى (0) هي الأكثر حمضية.
- المحاليل المتعادلة: تكون قيم (pH) لها تساوي (7).
- المحاليل القاعدية: تكون قيم (pH) لها أكبر من (7)، والمحاليل الأقرب إلى (14) هي الأكثر قاعدية.
الكاشف العام
Universal Indicator
يمكن قياس قيمة الرقم الهيدروجيني (pH) للمحاليل عملياً بإحدى طريقتين:
1- الكاشف العام
الكاشف العام: مزيج من عدّة كواشف يكون في صورة سائل أو أشرطة ورقية، ويُستخدم في تقدير قيمة الرقم الهيدروجيني للمحلول الحمضي أو القاعدي. يرفق مع الكاشف العام دليل ألوان قياسي أحياناً، يكون ملصقاً على العلبة التي يوجد فيها.
2- جهاز قياس الرقم الهيدروجيني
جهاز مقياس الرقم الهيدروجيني: جهاز يُستخدم لقياس الرقم الهيدروجيني في المختبرات، وفي العديد من الصناعات الكيميائية التي تعتمد على حمضية المحاليل وقاعديتها.
أسئلة المحتوى وإجاباتها
الكواشف والرقم الهيدروجيني
أتحقق صفحة (18):
ما أنواع الكواشف؟ أذكر مثالاً على كلّ منها.
- صناعية، مثل ورق تباع الشمس.
- طبيعية، مثل محلول الشاي ومنقوع الملفوف الأحمر.
تجربة صفحة (18):
تصنيف الكواشف
التحليل والاستنتاج:
1- أقارن بين منقوع الملفوف الأحمر وورق تباع الشمس من حيث: مصدر كل منهما، وتأثير إضافة الحمض والقاعدة في لونهما.

2- أفسر: أستخدم عينة ضابطة في التجربة.
أستخدم عينة ضابطة في التجربة؛ لأنها تعدّ مرجعاً لمقارنة لون المحلول المراد اختباره، بلون المحاليل المحدد نوعها حمضية أم قاعدية.
أتحقق صفحة (19):
ما المقصود بالرقم الهيدروجيني pH ؟
الرقم الهيدروجيني هو مقياس لحمضية أو قاعدية المحاليل، ويعبر عنه بتدريج رقمي من (14-0).
أفكر صفحة (20):
ما الأسباب التي تؤدي إلى تغير قيمة pH لدم الإنسان؟
هنالك أسباب متعددة تؤدي إلى تغير قيمة pH لدم الإنسان، منها بعض الحالات المرضية كالأمراض التنفسية، كما أن بعض الأدوية تسبب تغير قيمة الرقم الهيدروجيني للدم.
أتحقق صفحة (20):
أفسر لمَ يُعدّ جهاز مقياس الرقم الهيدروجيني، أكثر دقة من الكاشف العام.
يُعدّ جهاز مقياس الرقم الهيدروجيني، أكثر دقة من الكاشف العام؛ لأنه يحدد درجة حمضية المحلول ومدى ملاءمة استخدامه في مجال ما.
تجربة صفحة (21):
استخدام الكاشف العام
التحليل والاستنتاج:
1- أرتب المواد تصاعدياً حسب قيم pH .
حمض الهيدروكلوريك المخفف، الخل، عصير الليمون، ماء مقطر، محلول مسحوق الخبيز، محلول منظف الزجاج، محلول هيدروكسيد الصوديوم.
2- أصنّف المواد إلى حمضية وقاعدية ومتعادلة.

3- أقارن بين الكاشف العام والكواشف الأخرى.
الكاشف العام يحدد درجة حمضية أو قاعدية المحلول.
أسئلة مراجعة الدرس الثاني
الكواشف والرقم الهيدروجيني
السؤال الأول:
أفسّر. تُستخدم الكواشف للتمييز بين الحموض والقواعد.
السؤال الثاني:
أصنف المحاليل الآتية إلى حمضية أو قاعدية أو متعادلة بناءً على قيم pH :
أ- المحلول (أ): pH = 3
ب- المحلول (ب): pH = 8
ب- المحلول (د): pH = 7
السؤال الثالث:
أستنتج مستعيناً بقيم pH على تدريج الرقم الهيدروجيني في الشكل المجاور، أيّ الجمل الآتية صحيحة وأيّها غير صحيحة؟
أ- المحاليل الأكثر حمضية؛ قيم pH لها تقترب من 7 .
ب- المحاليل الأكثر قاعدية؛ قيم pH لها أكبر من 7 .
ج- يمكن تحديد الرقم الهيدروجيني للمحلول؛ باستخدام ورقة تباع الشمس.
السؤال الرابع:
التفكير الناقد: عند اختبار عينة من الحليب باستخدام ورقة تباع الشمس الزرقاء بقي لونها أزرق، وعند ترك الحليب لمدة من الزمن وإعادة الاختبار، وجد أن لون ورقة تباع الشمس الزرقاء تحول إلى اللون الأحمر. ما توقعاتي للتغيرات التي حدثت للحليب؟
تطبيق الرياضيات
مستعيناً بقيم pH على تدريج الرقم الهيدروجيني في الشكل السابق، أحسب مقدار الرقم الهيدروجيني pH لمحلول ما، علماً بأن مقداره يقل عن مثلي الرقم الهيدروجيني للماء بثلاثة أمثال الرقم الهيدروجيني لثمرة ليمون.
الإثراء والتوسّع
أزهار نبات القرطاسيا
تختلف ألوان أزهار نبات القرطاسيا تبعًا لدرجةِ حُموضة التربة، وقد استفاد المزارعونَ مِنْ هذه الظاهرة في إنتاج هذا النباتِ بألوان أزهار مختلفة؛ وذلك بإضافة مواد تعمل على تغيير قيمة الرقم الهيدروجيني للتربة التي ينبتُ فيها، فغيّروا لونَها مِنَ الزهري إلى الأزرق بناءً على امتصاص النبتة للمادة المضافة. أنظر الشكل (15).
أبحــث فــي مصادر المعرفة المتاحة، عــن المـواد التي يمكنني إضافتها للتربـة لإنتاج أزهار القرطاسيا ذاتِ اللون الزهري أو الأزرق، وأتعاون مع زملائي على زراعة أزهار القرطاسيا بألوانها المختلفة في حديقة مدرستي.
يتصف نبات القرطاسيا بأزهاره التي تتوضع في كتل كروية على شكل باقة عديمة الرائحة. ويمكن التحكّم بلون الأزهار عن طريق التحكم بدرجة حموضة التربة التي ينمو فيها. فقد وجد أنه يُمكن إضافة سلفات الألمنيوم مع مياه الري لتصبح التربة قاعدية؛ وبذا يتغيّر لون أزهار النبات ليصبح أزرق.
أنظر إلى الملف المرفق والذي يبين كيف يمكن تتغير لون أزهار نبات القرطاسيا من كتاب الكيمياء للصف الثاني عشر.
استقصاء علمي
تأثير المطر الحمضي في إنبات البذور
سؤال الاستقصاء:
تحتاج عملية إنبات البذور إلى الماء الذي تمتصه الجذورُ مِنَ التربة، ومن أهم مصادره مياه الأمطار التي تُعدُّ مِنَ المحاليل الحمضية الضعيفة؛ لأنها تحتوي على غاز ثاني أكسيد الكربون CO الذي يتفاعل مع بخار الماء في الهواء الجوي فيتكونُ حَمضُ الكربونيك، وتزداد حمضية ماء المطر بانخفاض قيمة الرقم الهيدروجيني pH فهل يؤثر التغير في قيمة الرقم الهيدروجيني للمياه في عملية إنبات البذور ؟
التحليل والاستنتاج والتطبيق
1- أفسّر استخدامي ملوّنَ طعام في أنبوب الاختبار (1) في الجزء (A)؟
استخدم الصبغة الملوّنة لتوضيح الملاحظة؛ لأنّ محلول الخل الأبيض شفّاف، ولون المحاليل يختلف باختلاف التركيز .
2- أحدّدُ المتغترات التابعة والمتغيّرات المستقلة في التجربة في الجزء (A) والجزء (B)؟
المتغيرات المستقلة في الجزء (A): درجة الحرارة وحجم المحلول، والتابعة هي الرقم الهيدروجيني. المتغيّرات المستقلة في الجزء (B): نوع البذور وحجم المحلول، والتابعة هي معدل إنبات البذور.
3- أُقدم دليلًا على حدوث عملية إنبات البذور.
الدليل على إنبات البذور ظهور الجذور للبذور.
4- ماذا تمثل المحاليل التي أضفتها للبذور ؟
مياه المطر.
5- أستخدم الأرقام: أحسبُ النسبة المئوية للبذور التي حدثت لها عملية إنبات في كُلِّ علبة،
وأُدوّنُ نتائجي.
تحقق من حسابات الطلبة للنسب المئوية وفقا لنتائجهم.
6- أُمثْلُ بيانيًا العلاقة بين قيمة الرقم الهيدروجيني (pH) للمحلول، والنسبة المئوية للبذور التي حدث لها إنبات.
تكون العلاقة عكسية بين معدل إنبات البذور وقيمة الرقم الهيدروجيني (كلّما قل الرقم الهيدروجيني للماء الذي تمتصه الجذور، زادت حمضية التربة فيقل معدل انبات البذور.
7- أُقارن نتائجي بصحة الفرضية التي كوّنتها.
وافقت نتائجي توقعاتي وثبت بالتجربة العملية أنّ الرقم الهيدروجيني يؤثر في إنبات البذور، وأنه كلّما قل الرقم الهيدروجيني (زادت حمضية مياه المطر)، قل معدل إنبات البذور.
إجابات أسئلة مراجعة الوحدة
السؤال الأول:
أكتب المفهوم العلمي المناسب لكل جملةٍ من الجمل الآتية:
- تعرف المواد التي يبدأ اسمها بهيدروكسيد: ( القواعد ).
- سبب تكون الصواعد والهوابط في الكهوف الجيرية، هو: ( المطر الحمضي ).
- محاليل يتغير لونها تبعاً لنوع المحلول الذي توجد فيه: ( الكواشف ).
- مقياس يُستخدم لتحديد حمضية أو قاعدية المحاليل: ( الرقم الهيدروجيني ).
- مواد تحضر صناعياً، وتُستخدم للتمييز بين الحموض والقواعد: ( كوشف صناعية ).
- مزيج من الكواشف يتغير لونه بتغير قيم pH التي تتراوح بين (14-0): ( الكاشف العام ).
السؤال الثاني:
أختار رمز الإجابة الصحيحة في ما يأتي:
1- إحدى المواد الآتية تغير لون ورقة تباع الشمس الحمراء إلى اللون الأزرق:
أ- ملح الطعام.
ب- سائل التنظيف.
ج- الخل.
د- الشاي.
2- الخاصية التي تشترك فيها محاليل الحموض والقواعد، هي:
أ- طعمها حامض.
ب- ملمسها صابوني.
ج- موصلة للتيار الكهربائي.
د- آكلة لبعض الفلزات.
3- معظم المواد التي تُستخدم في صناعة مواد التنظيف، هي:
أ- قاعدية.
ب- حمضية.
ج- أملاح.
د- متعادلة.
4- محلول الحمض الذي يُسهم في عملية هضم الطعام في المعدة، هو:
أ- حمض النيتريك.
ب- الكبريتيك.
ج- الهيدروكلوريك.
د- الخل.
5- يشير الرمز المجاور عند وجوده على ملصقات إحدى المواد إلى أنها:
أ- سامة.
ب- قابلة للاشتعال.
ج- كاوية للجلد.
د- تسبب الجروح.
6- السبب الرئيس لحدوث المطر الحمضي:
أ- النفايات الناتجة من الطاقة النووية.
ب- الانسكابات من مصانع المواد الكيماوية.
ج- الغازات الناتجة من احتراق الوقود الأحفوري.
د- الغازات المنبعثة من علب المعطرات الجوية.
7- قيمة pH للماء النقي، تساوي:
أ- 3
ب- 0
ج- 7
د- 9
8- يُصنف محلول مادة ما، قيمة pH له = 14 بأنه:
أ- مادة قاعدية.
ب- مادة حمضية.
ج- مادة متعادلة.
د- مطر حمضي.
9- الجهاز المستخدم في قياس درجة حموضة ماء المطر بدقة، هو:
أ- الميزان الزئبقي.
ب- مقياس درجة الحرارة.
ج- الميزان الحساس.
د- مقياس الرقم الهيدروجيني.
10- عند سقوط قطرات من عصير الليمون على سطح من الصخر الجيري، ينتج غاز:
أ- H2
ب- O2
ج- CO2
د- N2
السؤال الثالث:
المهارات العلمية
1- أكمل خريطة المفاهيم الآتية:

2- أصنف المواد الافتراضية (س، ص، ع، ل) إلى حمض أو قاعدة؛ مستعيناً بالمعلومات الواردة في الجدول الآتي:

3- أفسّر الظواهر الآتية بناءً على مفهومي للحموض والقواعد والكواشف:
أ- تستخدم مادة قاعدية في صناعة معجون الأسنان.
للتخلص من المواد الحمضية التي تبقى بعد تناول الطعام بين الأسنان، التي يمكن أن تسبب نخر الأسنان.
ب- تكون الكهوف الجيرية، مثل مغارة برقش في الأردن.
بسبب المطر الحمضي الذي يتفاعل مع كربونات الكالسيوم، ويتصاعد منها غاز ثاني أكسيد الكربون، ما أدى إلى وجود الكهوف الجيرية.
ج- ارتداء القفافيز في أثناء استخدام مواد التنظيف.
لأن مواد التنظيف تدخل في تركيبها مواد قاعدية وهي كاوية للجلد.
4- أصف دور مضاد الحموضة في تخفيف الحموضة في المعدة.
يُستخدم هيدروكسيد المغنيسيوم مضاداً لحموضة المعدة، إذ إنّه مادة قاعدية تتفاعل مع الزيادة في المحلول الحمضي في المعدة وتعادله، ما يخفف من أعراض سوء الهضم الحمضي.
5- ينتج من احتراق الفحم الحجري في بعض محطات توليد الطاقة غاز ثاني أكسيد النيتروجين. أصف تأثير هذه العملية في المباني القريبة من هذه المحطات.
نتيجة احتراق الوقود الأحفوري (مشتقات النفط) تنتج غازات مثل NO2 التي تتفاعل مع ماء المطر الحمضي، وعند سقوطه على المباني المكونة من الحجر الجيري أو الرملي التي تتكون من كربونات الكالسيوم CaCO3 ؛ تعمل على إذابة جزء منها ويتصاعد غاز CO2 وتصبح المباني مشوهة.
6- مستعيناً بالشكل والجدول الآتيين، أجيب عن الأسئلة الآتية:
أ- أستنتج: ما المواد التي استخدمها في حياتي اليومية تمثل الرموز (أ، ب، ج، د، هـ)؟

ب- أتوقع: ما المواد الغذائية التي يمكن تناولها للتخفيف من حموضة المعدة؟
يمكن استخدام البروكلي لتخفيف حموضة المعدة.
ج- أتوقع: ماذا يمكن أن يحدث لسطح الرخام إذا قطعت الليمون عليه باستمرار؟
تقطيع الليمون على سطح الرخام باستمرار يؤدي إلى تلفه وتشوه سطحه وتكوين حفر فيه؛ نتيجة تفاعل الحمض مع كربونات الكالسيوم المكون الكيميائي للرخام، ويتصاعد غاز CO2 ، فتتكون الحفر ويتشوه الرخام.